Исследование
процесса окисления активного
древесного
угля кислородом воздуха
Еранкин С.В. (Институт органического синтеза УрОРАН, г. Екатеринбург, Россия),
Гиндулин И.К., Юрьев Ю.Л. (УГЛТУ, г. Екатеринбург, Россия) tradeek@mail.ru
Research process of oxidation active charcoal by
oxygen of air
В настоящее время перед лесопромышленным комплексом достаточно остро стоит проблема безотходных технологий. Одним из решений является термохимическая переработка отходов лесопиления с получением ценных продуктов на базе древесного угля. Это направление ранее сдерживалось проблемой экологической опасности производства, которая в последнее время успешно решена. Производство древесного угля на территории РФ развивается высокими темпами. Одним из перспективных направлений переработки древесного угля является получение модифицированных продуктов с развитой нанопористой структурой, в частности – окисленного угля.
Окисленный уголь – это форма твердого углерода, содержащая на своей поверхности кислородсодержащие функциональные группы. Для производства окисленных углей в промышленных масштабах возможно использование в качестве сырья как ископаемых (бурых или каменных) углей, так растительных углей. Древесные угли имеют несомненное преимущество перед минеральными углями – развитую пористую структуру, что облегчает процессы активации и окисления углей и позволяет получать продукт с более высокой сорбционной емкостью.
На поверхности окисленных углей существуют разнообразные кислородсодержащие функциональные группы. Та часть этих групп, которая обладает кислотными свойствами, имеет разную химическую природу и весьма различную способность к ионизации в водных растворах. Вследствие этого окисленные угли являются полифункциональными катионообменниками с широким диапазоном изменения кислотных свойств, ответственных за способность к ионному обмену протогенных групп. На поверхности окисленных углеродных сорбентов были обнаружены карбоксильные группы, лактонные и лактольные структуры, которые при подходящих условиях могут преобразовываться в карбоксильные группы, фенольные и спиртовые гидроксилы, карбонилы (карбоксилов, хиноидные, альдегидные, кетонные), гидроперекисные группы. Вследствие наличия на поверхности окисленного угля кислотных групп возможно замещение ионов водорода этих групп катионами металлов. При этом наблюдается эквивалентность ионного обмена (с поправкой на сорбцию анионов не окисленными участками поверхности угля), однако при сорбции ряда ионов, особенно склонных к комплексообразованию эквивалентность уже не наблюдается, что может быть связано с необменной сорбцией катионов, поглощенных частично закомплексованных форм. Наличие на поверхности окисленного угля большого числа различных кислотных группировок, содержащих координационно-ненасыщенные атомы кислорода, легкость перемещения электронов по цепи сопряженных связей создают предпосылки к тому, что при взаимодействии углей с отдельными катионами металлов будет происходить не просто обмен ионов водорода на соответствующие катионы, но и образование более или менее прочных поверхностных комплексов, в которых функциональные группы углей выступают в качестве лигандов. Эти обстоятельства и обуславливают ряд особенностей, отличающих обмен катионов на окисленном угле от обмена на других ионитах.
По способности поглощаться окисленным углем катионы можно расположить в такой ряд:
NH4+<Na+<Cs+<Mg2+<Cd2+, Mn2+<Ca2+, Zn2+, Fe2+<Ni2+, Al3+<Cr3+<Cu2+<Fe3+
На окисленных
углях во многих случаях при поглощении из смесей сорбция сильнее поглощаемых ионов
практически происходит так, как будто менее сорбируемый
ион в смеси просто отсутствует. Селективное поглощение
микрокомпонентов наблюдается в очень многих системах – при сорбции примесей
щелочноземельных, переходных и других многозарядных ионов из растворов солей и
гидроокисей щелочных металлов и аммония, следовых количеств бериллия, меди,
железа из растворов солей щелочноземельных металлов, примесей меди и железа из
растворов солей алюминия, цинка, кадмия и др. В отличие от окисленного угля, на
других ионитах наличие конкурирующих ионов сразу снижает сорбцию многих
ионов даже тогда, когда разделяемые ионы сильно
различались по поглотительной способности при сорбции из индивидуальных
растворов. Различия в прочности связи отдельных ионов с окисленным углем
настолько велики, что удается проводить количественное извлечение
микрокомпонентов при огромном избытке одноименно заряженных ионов, что
обусловило широкое применение окисленного угля для глубокой очистки различных
реактивов от микропримесей и других тонких химических разделений.
Получение окисленного древесного угля является многостадийным процессом и осуществляется в следующем порядке: пиролиз древесины, активация полученного древесного угля, окисление поверхности активного древесного угля. В процессе пиролиза происходит изменение пористой структуры древесной матрицы. Структура березовой древесины и полученного из нее березового угля-сырца показана на рисунках 1 и 2 соответственно.
Активация позволяет
получать угли с внутренней площадью поверхности до
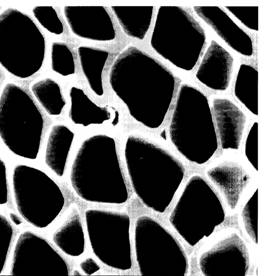
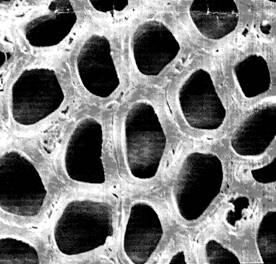
Рис.1 Структура березовой древесины Рис.2 Структура березового угля-сырца
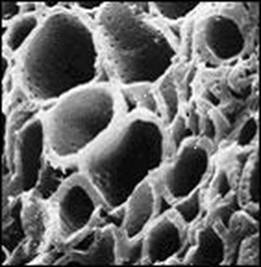
Рис.3 Структура растительного активного угля
Третьей, заключительной стадией получения древесного окисленного угля является собственно окисление поверхности активного древесного угля. Окисление угля очень медленно проходит на воздухе и при комнатной температуре. Получение углеродных сорбентов с катионообменными свойствами может быть осуществлено при обработке угля в газовой или жидкой фазе. При окислении угля происходит несколько параллельных процессов: каталитическое разложение окислителя, окислительно-восстановительное взаимодействие с углем с образованием поверхностных и фазовых окислов, а также частичное разрушение структуры с образованием веществ гуминового характера, которые в дальнейшем могут смываться в раствор. Полезным из этих процессов является только один – образование поверхностных окислов. Наиболее реакционноспособными на поверхности являются дефекты структуры, атомы на углах и гранях кристаллитов. Неактивированные и малоактивированные карбонизаты дают меньше товарного продукта, но окисляются намного лучше, чем активированные угли, что связано с первичным окислением алифатических фрагментов, а затем уже матрицы угля. Чем более упорядочена структура поверхности, тем труднее процесс образования поверхностных окислов.
Для создания оптимальной технологии требуется нахождение таких условий, в которых в наибольшей степени происходило бы поверхностное окисление с возможно меньшим расходом окислителя, энергии, обгаром угля и образованием гуминовых веществ.
Основные недостатки при окислении азотной кислотой – невысокая химическая устойчивость продукта в щелочных средах, образование гуминовых веществ, образование во время процесса окисления токсичных веществ.
При окислении гипохлоритом натрия получаются окисленные угли с вполне удовлетворительными характеристиками, но необходима отмывка для перевода окисленного угля в Н-форму и, как следствие, расход HCl и воды.
Окисление перекисью водорода приводит к образованию окисленных углей хорошего качества, не требует отмывки, но зачастую происходит разложение перекиси под каталитическим действием углерода без воздействия на поверхность угля, что приводит к непомерно большому расходу окислителя, соотношение по массе «перекись водорода : древесный активный уголь» может составлять до 700:1, в зависимости от исходного сырья и необходимой степени окисленности конечного продукта.
Наиболее предпочтительным является окисление воздухом, при котором возможно получение несколько различных по свойствам древесных окисленных углей. Трудностью данного метода является соблюдение оптимальных условий окисления. Отклонение от них приводит либо к высокому обгару угля, либо к получению продукта с низкой катионообменной емкостью.
Работами, проведенными на кафедре химической технологии древесины УГЛТУ, показано, что основными факторами, влияющими на выход и качество древесного окисленного угля при окислении воздухом, являются температура и продолжительность процесса окисления.
Зависимость величины обгара от температуры показана на рис. 4.
![]()
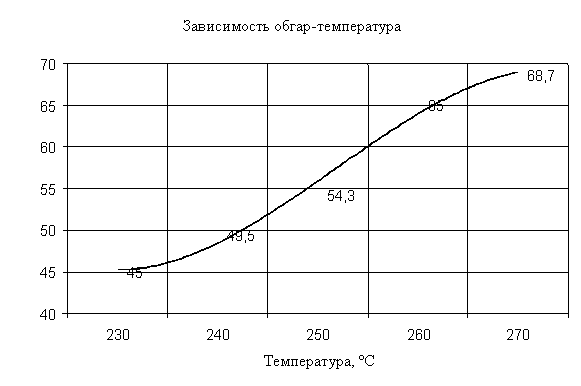
Рис.4 Зависимость
величины обгара от температуры
Из графика
видно, что с повышением температуры окисления с 230 до 2600С обгар увеличивается на 20%, т. е. возрастает от 45 до 65%
от загрузки.
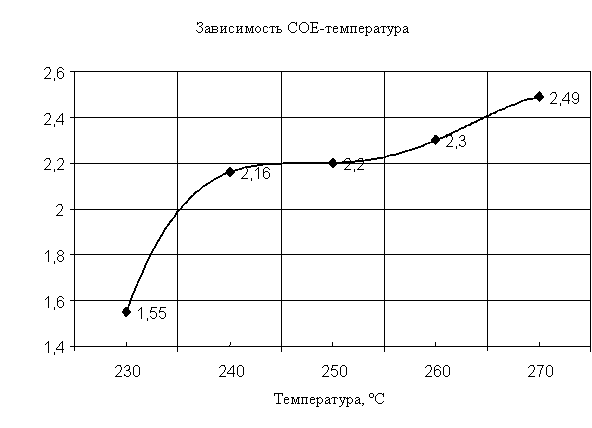
Одним из показателей, определяющих качество древесного окисленного угля является сорбционная общая емкость (СОЕ) по щелочи, которая отражает количество разнообразных кислородсодержащих функциональных групп. Чем больше значение СОЕ, тем больше кислородсодержащих функциональных групп. На рисунке 5 показана зависимость СОЕ от температуры.
Из рисунка 5 видно, что повышение температуры ведет к увеличению значения СОЕ. При температуре окисления ниже 240ºС получается продукт с низким значением СОЕ. В интервале температур 240…255 ºС величина СОЕ практически не изменяется. При температурах 260 ºС … 270 ºС происходит существенное увеличение значения СОЕ, но величина обгара в этих условиях превышает 60%.
Рис.5 Зависимость
СОЕ от температуры
![]()
По результатам работы можно сделать следующие выводы:
- Показано, что возможно получение окисленного угля с величиной СОЕ около 2 мг-экв/г путем окисления насыщенным воздухом при температуре не выше 270 ºС, до этого по литературным данным считалось, что для получения подобного продукта необходима температура около 400 ºС;
- Получены данные, необходимые для расчета кинетики процесса окисления АУ воздухом;
- По результатам эксперимента можно сделать вывод, что наиболее рационально проводить окисление при температуре 2400С. При этом получен продукт с величиной СОЕ более 2мг-экв./г при обгаре около 50%.